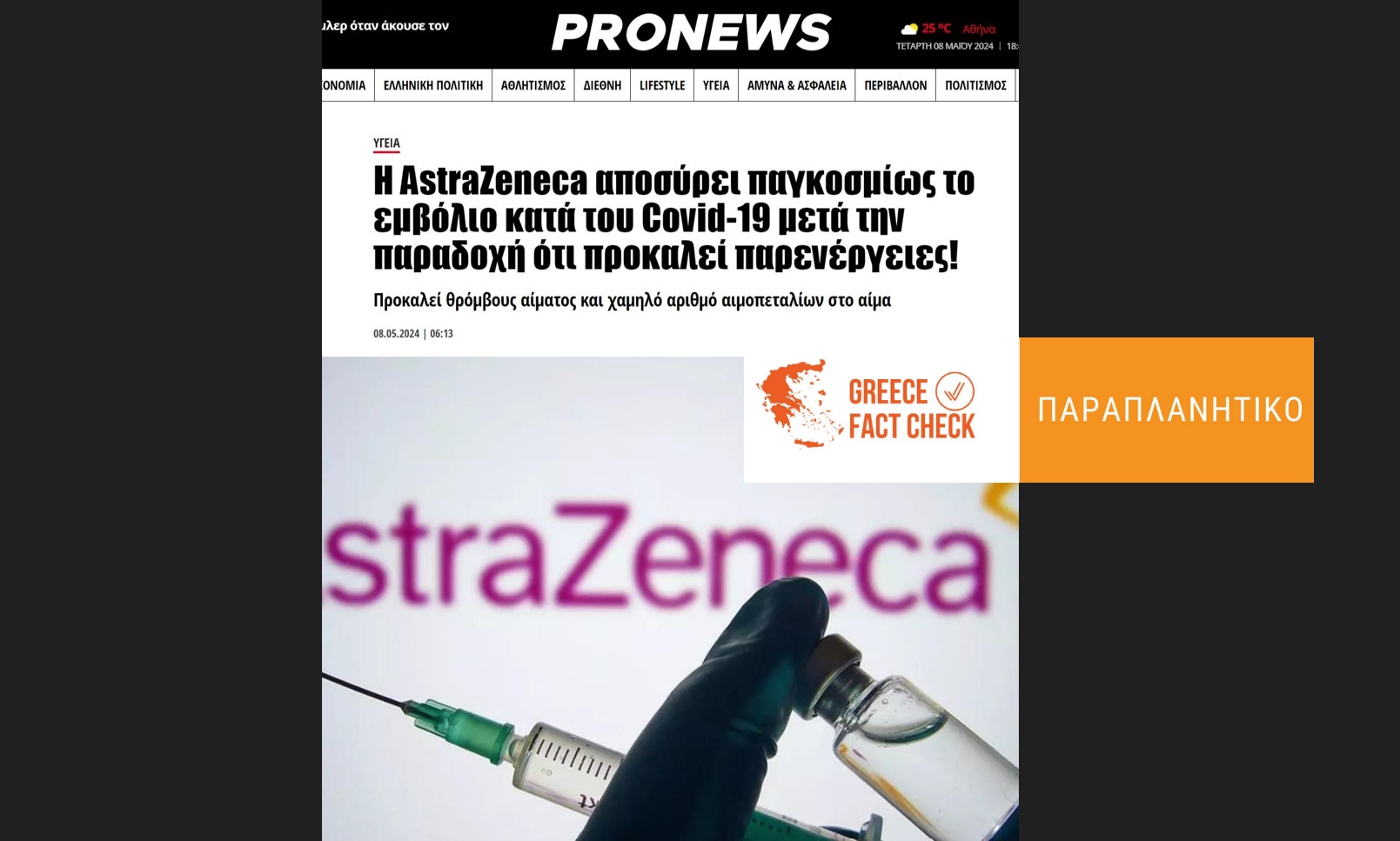
ΙΣΧΥΡΙΣΜΟΣ 1: Οι Ευρωπαϊκές αρχές απέσυραν το εμβόλιο της AstraZeneca λόγω παρενεργειών.
ΙΣΧΥΡΙΣΜΟΣ 2: Η Astra Zeneka απέσυρε το εμβόλιό της κατά της COVID-19 εξαιτίας των παρενεργειών του.
ΣΥΜΠΕΡΑΣΜΑΤΑ: Η διακοπή του εμβολίου Vaxzevria ήταν μια στρατηγική απόφαση της AstraZeneca που επηρεάστηκε από τη δυναμική της αγοράς και την απορρόφηση των εμβολίων και τη διαθεσιμότητα πιο επικαιροποιημένων και αποτελεσματικών εμβολίων, παρά ένα αντιδραστικό μέτρο λόγω αστοχιών σε θέματα ασφάλειας. Η απόσυρση από τις Ευρωπαϊκές αρχές ήρθε έπειτα από αίτημα της AstraZeneca.


Τι ισχύει
Το εμβόλιο της Astra Zeneca για τον κορωνοϊό σχεδιάστηκε από το Πανεπιστήμιο της Οξφόρδης. Το Vaxzevria αποτελείται από έναν άλλο ιό (της οικογένειας αδενοϊών) που έχει τροποποιηθεί ώστε να περιέχει το γονίδιο για την παραγωγή της πρωτεΐνης S από το SARS-CoV-2. Κυκλοφόρησε με τις ονομασίες Covishield και Vaxzevria. Μελέτες που διεξήχθησαν το 2020 έδειξαν ότι η αποτελεσματικότητα του εμβολίου είναι 76,0% στην πρόληψη της συμπτωματικής COVID-19 και αρχίζει στις 22 ημέρες μετά την πρώτη δόση και 81,3% μετά τη δεύτερη δόση (αφορούσαν το πρώτο στέλεχος). Σε πολύ σπάνιες περιπτώσεις (περίπου 1 στα 100.000 άτομα), το εμβόλιο έχει συσχετιστεί με αυξημένο κίνδυνο θρομβώσεων στο αίμα σε συνδυασμό με χαμηλά επίπεδα λευκοκυττάρων και αιμοπεταλίων [θρόμβωση με σύνδρομο θρομβοκυτταροπενίας (TTS)]. Σύμφωνα με τον Ευρωπαϊκό Οργανισμό Φαρμάκων, από τις 4 Απριλίου 2021, καταγράφηκαν συνολικά 222 περιπτώσεις θρόμβων μεταξύ 34 εκατομμυρίων ανθρώπων που είχαν εμβολιαστεί στον Ευρωπαϊκό Οικονομικό Χώρο (ποσοστό 0,0007%).
Το εμβόλιο κυκλοφόρησε για πρώτη φορά στο Ηνωμένο Βασίλειο στις 4 Ιανουαρίου του 2021 και στα πλεονεκτήματά του συνυπολογίζονταν η ανταγωνιστική τιμή και ότι ήταν εύκολο στη μεταφορά καθώς μπορούσε να αποθηκευτεί σε υψηλότερες θερμοκρασίες σε σχέση με τα υπόλοιπα. Τον Μάρτιο του 2021, ορισμένες ευρωπαϊκές χώρες ανέστειλαν τη χορήγηση του εμβολίου της AstraZeneca για προληπτικούς λόγους, μετά τις αναφορές για περιπτώσεις εμφάνισης θρομβώσεων σε εμβολιασθέντες. Η ρυθμιστική αρχή της Ευρωπαϊκής Ένωσης διενήργησε επείγουσα επανεξέταση καταλήγοντας στο συμπέρασμα ότι το εμβόλιο ήταν ασφαλές για χρήση και ότι δεν συνδέεται με αύξηση του συνολικού κινδύνου θρομβοεμβολικών επεισοδίων ή θρόμβων αίματος.
Το εμβόλιο δεν είναι πλέον σε παραγωγή λόγω της υποχώρησης της πανδημίας Covid-19 και της διαθεσιμότητας επικαιροποιημένων εμβολίων. Η AstraZeneca απέσυρε τις άδειες χρήσης για το εμβόλιο από την ευρωπαϊκή αγορά στις 27 Μαρτίου 2024, και παγκοσμίως από τις 7 Μαΐου 2024. Η Ευρωπαϊκή Επιτροπή ενέκρινε το αίτημα του κατασκευαστή να αποσύρει το εμβόλιο λόγω πλεονάσματος επικαιροποιημένων εμβολίων, το οποίο μείωσε τη ζήτηση για το Vaxzevria.
Επομένως, σχεδόν τρία χρόνια μετά, η ΑstraZeneca ανακοίνωσε πως αποσύρει το εμβόλιο κατά του κορονοϊού, με το οποίο εμβολιάστηκαν εκατομμύρια πολίτες για το αρχικό στέλεχος ανά τον κόσμο, λόγω “πλεονάσματος διαθέσιμων επικαιροποιημένων εμβολίων” μετά την πανδημία. Κατόπιν, ο Ευρωπαϊκός Οργανισμός Φαρμάκων (EMA) ανακοίνωσε:
Η εξουσιοδότηση μάρκετινγκ (σ.σ. άδεια χρήσης) για το Vaxzevria (SRD) αποσύρθηκε κατόπιν αιτήματος του κατόχου μάρκετινγκ-εξουσιοδότησης. σ.σ. AstraZeneca.
Με απλά λόγια, η ανάκληση της εξουσιοδότησης του εμβολίου Vaxzevria προήλθε από αίτηση της κατασκευάστριας εταιρίας ΑstraZeneca και όχι κάποιας “Ευρωπαϊκής αρχής”.
Η AstraZeneca έχει μηνυθεί από περισσότερα από 50 φερόμενα θύματα και συγγενείς στο Ανώτατο Δικαστήριο του Ηνωμένου Βασιλείου, ζητώντας συνολικά 100 εκατομμύρια στερλίνες αποζημίωση. Η AstraZeneca έχει παραδεχτεί ότι το εμβόλιο μπορεί, σε πολύ σπάνιες περιπτώσεις, να προκαλέσει θρομβώσεις, αλλά αρνείται ότι το εμβόλιο ευθύνεται για τις συγκεκριμένες βλάβες που ισχυρίζονται οι ενάγοντες. Σύμφωνα με τα σχετικά δημοσιεύματα στον βρετανικό Τύπο, η φαρμακευτική εταιρεία προτίθεται να αντιμετωπίσει στο δικαστήριο τις εις βάρος της κατηγορίες αλλά έχει παραδεχτεί σε νομικό έγγραφο, το οποίο κατατέθηκε στο δικαστήριο τον Φεβρουάριο, πως το εμβόλιο που παρασκεύασε για τη νόσο Covid – 19 «ενδέχεται σε πολύ σπάνιες περιπτώσεις να προκαλέσει TTS – θρόμβωση με σύνδρομο θρομβοκυτταροπενίας». Πρόκειται για μια σοβαρή πάθηση κατά την οποία παρουσιάζονται θρόμβοι αίματος στον εγκέφαλο ή σε άλλα μέρη του σώματος ενώ συνδέεται και με χαμηλά επίπεδα αιμοπεταλίων.
Θα πρέπει να αναφερθεί πως η πιθανή παρενέργεια που προκαλεί TTS σε λιγότερα από 1 στα 100.000 άτομα, δεν ήταν κάτι που έμεινε κρυφό. Σε φυλλάδιο του εμβολίου της AstraZeneka, αναφερόταν αυτό το πιθανό ενδεχόμενο:


Σύμφωνα με το Fact-Check Cyprus, λόγω της δημόσιας ανησυχίας και της διαθεσιμότητας άλλων εμβολίων, ορισμένες χώρες σταδιακά κατάργησαν ή περιόρισαν τη χρήση του εμβολίου AstraZeneca, ευνοώντας τα εμβόλια mRNA όπως αυτά της Pfizer-BioNTech και της Moderna. Το εμβόλιο AstraZeneca συνέχισε να χρησιμοποιείται, ιδιαίτερα όπου οι απαιτήσεις αποθήκευσης και χειρισμού του προσέφεραν υλικοτεχνικά πλεονεκτήματα.
Συμπέρασμα
Η διακοπή του εμβολίου Vaxzevria ήταν μια στρατηγική απόφαση της AstraZeneca που επηρεάστηκε από τη δυναμική της αγοράς και την απορρόφηση των εμβολίων και τη διαθεσιμότητα πιο επικαιροποιημένων και αποτελεσματικών εμβολίων, παρά ένα αντιδραστικό μέτρο λόγω αστοχιών σε θέματα ασφάλειας. Η απόσυρση από τις Ευρωπαϊκές αρχές ήρθε έπειτα από αίτημα της AstraZeneca.